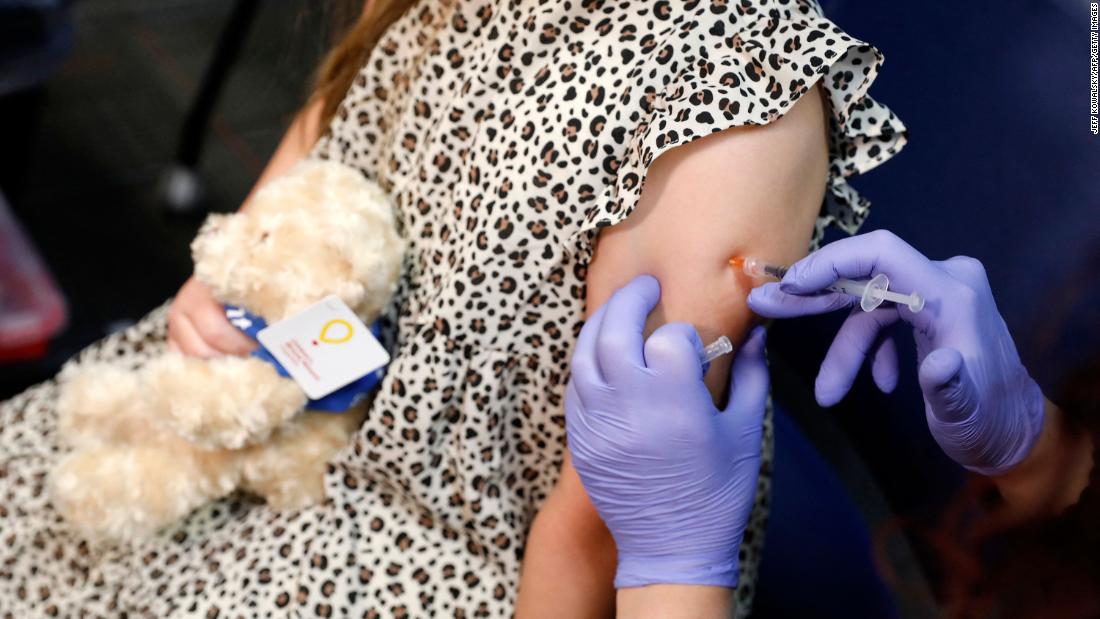
Дети в возрасте до 5 лет — около 18 миллионов человек — являются единственной возрастной группой в США, которая не имеет права на прививку от Covid-19.
Вакцина Moderna разрешена для использования у взрослых, но во вторник консультанты обсудят включение детей в возрасте от 6 до 17 лет; в среду они рассмотрят вопрос о распространении разрешения на младенцев и детей в возрасте от 6 до 5 месяцев.
На встречах во вторник и среду члены VRBPAC проголосуют за то, перевешивают ли преимущества вакцин Moderna и Pfizer/BioNTech риски для детей младшего возраста.
Что будет дальше после встречи консультантов по вакцинам
После того, как консультанты FDA по вакцинам проголосуют, агентство рассмотрит свое решение и взвесит, следует ли ему разрешать вакцины.
Тем не менее, прививки не могут быть сделаны до тех пор, пока консультанты Центров по контролю и профилактике заболеваний США не проголосуют за то, рекомендовать ли их, и директор CDC доктор Рошель Валенски не подпишет рекомендацию.
Белый дом заявил, что вакцины для самых маленьких детей могут начать на следующей неделе.
Внедрение вакцин для этой группы может быть таким же, как и для детей старшего возраста, поскольку кабинеты педиатров будут играть важную роль в оказании помощи в проведении прививок.
Некоторые аптечные клиники также готовятся ввести больше вакцин.
«Мы планируем предоставить вакцины против COVID-19 детям в возрасте от 18 месяцев до четырех лет в нашей национальной сети из 1100 отделений MinuteClinic после того, как FDA и CDC предоставят рекомендации и будут получены запасы», — заявил представитель CVS Мэтт Бланшетт в заявлении по электронной почте в понедельник. .
«Наши клиницисты MinuteClinic, состоящие из сертифицированных семейных медсестер, младших врачей и медсестер, имеют значительный опыт вакцинации молодого населения, а также частные кабинеты для осмотра, что облегчит процесс для детей, родителей и опекунов». говорится в заявлении.
Дети до 5 лет обычно имеют более низкие показатели заболеваемости Covid-19, чем другие возрастные группы. Но в первую неделю июня уровень госпитализации среди этих детей был немного выше, чем среди взрослых в возрасте до 50 лет, и в четыре раза выше, чем среди других детей.
данные Pfizer
Люди в возрасте 5 лет и старше уже имеют право на получение двухдозовой вакцины против Covid-19 от Pfizer/BioNTech и бустерной дозы, но на встрече в среду члены VRBPAC обсудят, добавлять ли детей младшего возраста к разрешению на экстренное использование.
Согласно справочному документу, трехдозовая вакцина против Covid-19 от Pfizer для детей младше 5 лет, по-видимому, безопасна и в испытаниях вызывает иммунный ответ, сравнимый с реакцией у пожилых людей.
Одно испытание включало более 4500 детей в возрасте от 6 до 23 месяцев и от 2 до 4 лет. Некоторым сделали три прививки по 3 микрограмма, при этом вторую прививку сделали через три недели после первой, а третью прививку сделали как минимум через восемь недель после второй. Остальные получили плацебо.
В справочном документе FDA говорится, что вакцина Pfizer для этой возрастной группы вызывала ответы, сравнимые с теми, которые наблюдались у людей в возрасте от 16 до 25 лет. В исследовании было недостаточно случаев Covid-19, чтобы установить эффективность вакцины, но FDA отметило, что эта вакцина, как известно, менее защищает от варианта Omicron.
Предварительный анализ показал, что эффективность вакцины для детей младше 5 лет составляет 80,4%, при этом три случая Covid-19 были в группе вакцины и семь — в группе плацебо. Все случаи произошли, когда в США доминировал вариант Омикрон.
«Учитывая неопределенность пандемии COVID-19 и вероятность продолжения передачи SARS-CoV-2 в последующие месяцы, развертывание вакцины для детей в возрасте от 6 месяцев до 4 лет, вероятно, окажет благотворное влияние на COVID-19. связанные с этим заболеваемость и смертность в этой возрастной группе», — говорится в анализе FDA.
Случаев анафилаксии не было. Также не было зарегистрировано ни одного случая миокардита или перикардита — воспаления сердечной мышцы и тканей, окружающих сердце, — среди более чем 3000 реципиентов вакцины в ходе испытания, но это была недостаточно большая группа, чтобы исключить риск. .
Наиболее частыми побочными реакциями у детей в возрасте от 6 до 23 месяцев были раздражительность, сонливость, отсутствие аппетита и болезненность в месте инъекции. У детей в возрасте от 2 до 4 лет наиболее частыми побочными реакциями были боль или покраснение в месте инъекции и утомляемость.
Неясно, как долго вакцина будет эффективна; агентство отметило, что период оценки был ограничен и что, как известно, защита со временем ослабевает в пожилом возрасте. Агентство также заявило, что «вероятно, что в дополнение к первичной серии из трех доз потребуется бустерная доза для повышения надежности, широты и продолжительности защиты».
Данные Модерны
Согласно справочным документам FDA, иммунный ответ и профиль безопасности вакцины Moderna Covid-19 также благоприятны для самых маленьких детей.
Члены VRBPAC обсудят вакцину Moderna во вторник и среду, оценивая, следует ли ее разрешить для более молодого возраста.
В испытаниях, в которых приняли участие более 6000 детей в возрасте от 6 месяцев до 6 лет, ученые Moderna обнаружили, что две дозы вакцины по 25 мкг, введенные с интервалом в 28 дней, вызывают такой же иммунный ответ, как и серия двух доз вакцины у взрослых в возрасте от 18 до 25 лет. .
У детей и подростков в возрасте от 6 до 17 лет Moderna обнаружила, что две дозы ее вакцины обеспечивают такой же иммунный ответ, как две дозы у взрослых.
Было также установлено, что вакцина безопасна для всех возрастных групп, при этом побочные реакции описываются как «в основном от легкой до умеренной степени тяжести, как правило, кратковременные» и чаще возникают после второй дозы, чем после первой, согласно документу. Боль в месте инъекции была наиболее часто сообщаемой побочной реакцией. Что касается серьезных нежелательных явлений, то в документе они описываются как нечастые и не вызывают никаких опасений. О смертельных случаях не сообщалось.
Хотя не было известных случаев миокардита или перикардита, связанных с вакциной, это признано одним из известных рисков, и о нем сообщалось в основном у мужчин в возрасте от 18 до 24 лет.
FDA не требовало от производителей вакцины предоставления данных об эффективности вакцины для разрешения на экстренное использование для детей младшего возраста, но вакцина Moderna, по оценкам, на 93,3% эффективна против симптоматического Covid-19 среди подростков в возрасте от 12 до 17 лет, когда исходный коронавирус и Альфа вариант был доминирующим.
По оценкам, вакцина на 76,8% эффективна против симптоматического Covid-19 для детей в возрасте от 6 до 11 лет, когда преобладал дельта-вариант. Однако FDA также отметило, что для детей этой возрастной группы «эффективность вакцины не может быть надежно определена из-за небольшого числа случаев COVID-19, зарегистрированных во время исследования».
Вакцину тестировали в то время, когда доминировал вариант Омикрон. По оценкам, он на 36,8% эффективен против симптоматического Covid-19 для детей в возрасте от 2 до 5 лет и на 50,6% защищает детей в возрасте от 6 до 23 месяцев.
Согласно справочному документу FDA, оценки эффективности вакцин «в целом соответствовали» тем, что наблюдались у взрослых.
Аманда Сили из CNN, Дейдра Макфиллипс и Джейми Гамбрехт внесли свой вклад в этот отчет.